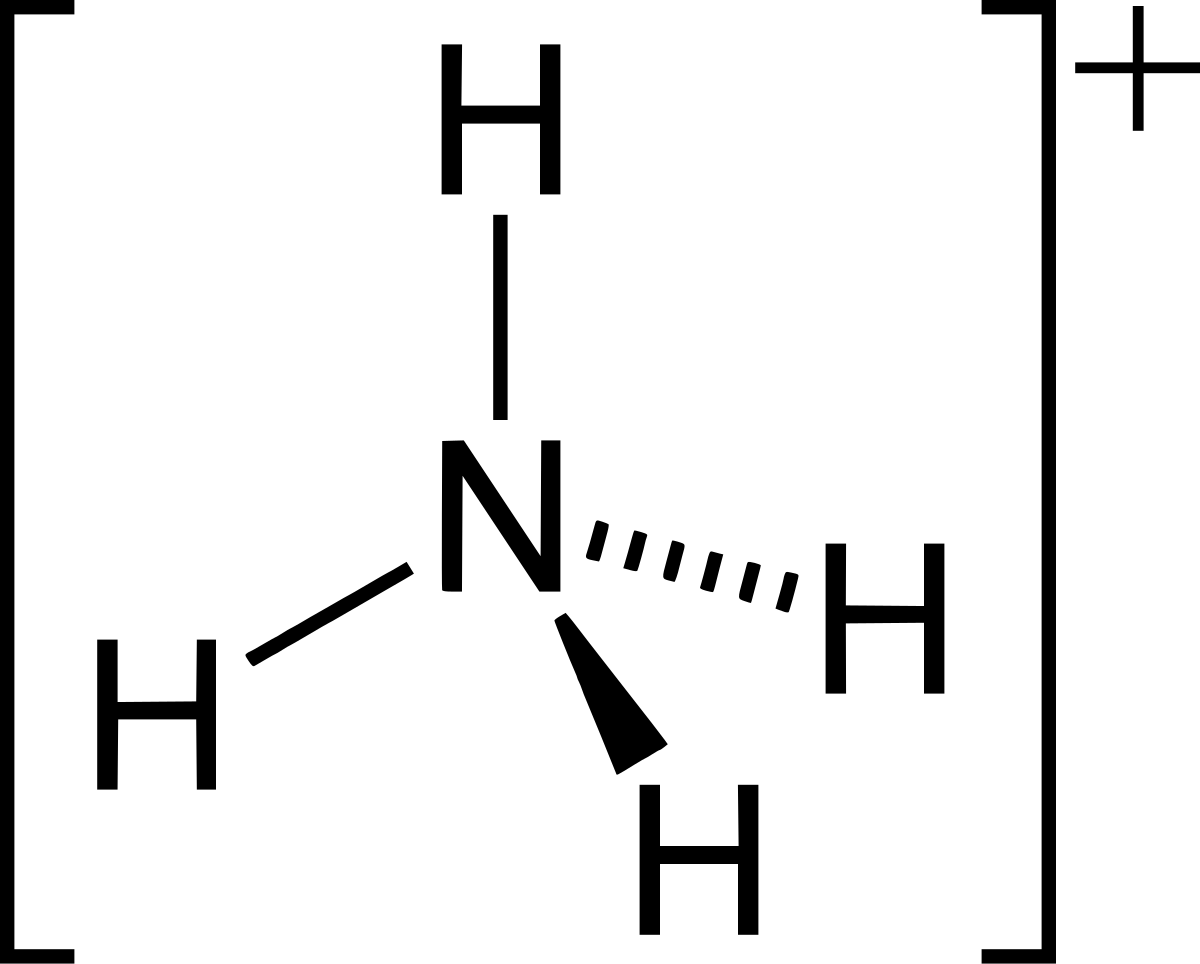
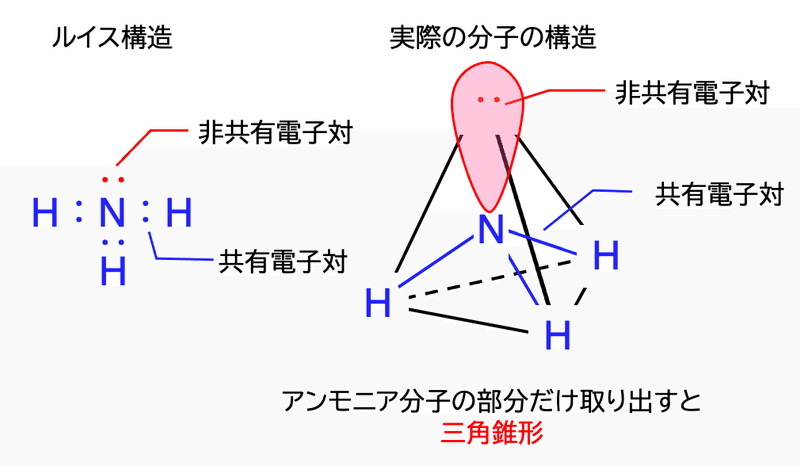
アンモニアにおける三角錐形幾何配置 アンモニア中の窒素原子は5個の価電子と3つの水素原子との結合を持ち、オクテット則を満たしている。 この結果、それぞれの結合角が cos −1 (− 1 / 3) ≈ 1095° と等しい正四面体の幾何配置がもたらされるだろう。 しかしながら、3つの水素原子は孤立図1 アンモニア分子構造の模式図 図2 アンモニア分子の反転遷移 アンモニア分子(nh 3;アンモニアの性質 アンモニアの用途 分子式 NH 3 気体密度 06 kg/m3 液体密度 0680 kg/L 液化圧力 846 kPa エネルギー密度 1849 kJ/kg 溶解度 90 g (100 mL of water at 0̊C ) 刺激臭を持った無色の気体 肥料用 →無水ガスや水溶液として土壌へ – 硝酸塩、硫酸塩、ニリン酸塩など
アンモニウム Wikipedia
アンモニア 構造 分子
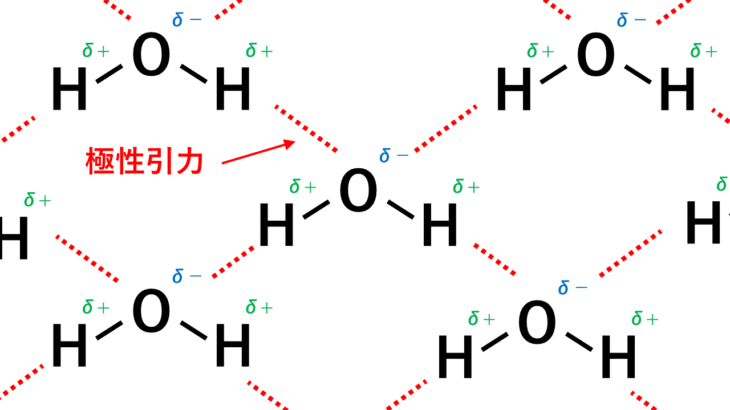
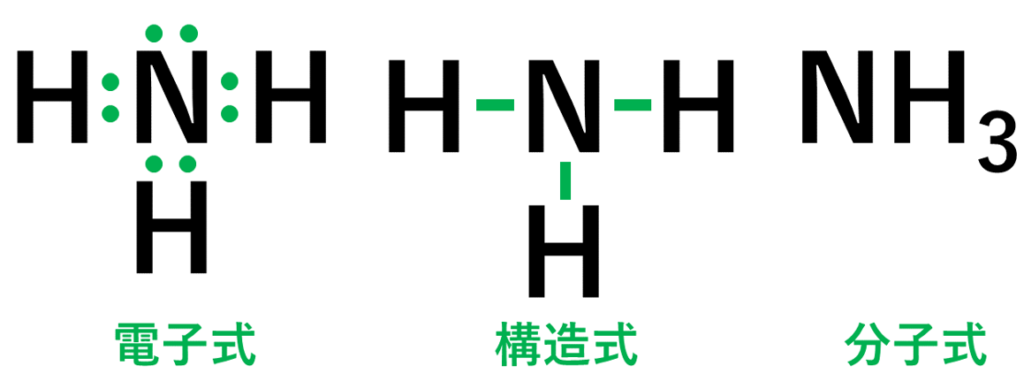
アンモニア 構造 分子-アンモニア分子の立体構造を混成軌道の考え方を用いて説明し 構造式 分子の形 水素h 2 直線 水h 2 o 折れ線 アンモニアnh 3 三角錐 メタンch 4 正四面体 二酸化炭素co 2 直線 窒素n 2 直 :o=s→o: 電子式(b)に対応する構造式 のようになります。アンモニア( nh 3 ) 周期表第 15族の窒素( n )の水素化物であるアンモニアは,3つの共有電子対と 1つの非共有電子対を持つ。 水素と窒素の電気陰性度の差が比較的大きく,アンモニア分子は非対称の構造となるため,双極子が発生する。



Chem Chem Cher Ee Rhf 3 21gレベルにおけるアンモニアの構造最適化 振動解析
Jul 25, 19 · アンモニアをエネルギーキャリアとして利用するためには、アンモニアを窒素分子へと酸化し、同時にアンモニアに蓄えられた化学エネルギーを電気エネルギーなどの形に効率的に変換するアンモニアの触媒的酸化反応の開発が望まれている(図1)。理論計算により、1-ナフトール‐アンモニアクラスターのS 1状態では、n = 3まではナフ トールからアンモニアへプロトン移動していないnonESPT体が最安定構造となり、n = 4お よび5ではプロトン移動したESPT体が最安定構造となることがわかった。図にn = 4のS 1アンモニアの分子式・構造式・電子式・分子量・イオン式は? それでは、アンモニアの基礎的な物性について考えていきましょう。 アンモニアの分子式 まず、アンモニアの分子式は組成式と同じであり、 nh3 で表されます。
アンモニアボランはエタンの分子構造を採用している。bn間の距離は158(2) Åである。bh間とnh間の距離はそれぞれ115 と 096 Åである。 エタンが常温で気体であるのに対し構造(15)が存在する可能性は少ないと考えられるが, pヒドロキシフェニル核(12)の縮合型構造は複雑であろう たとえば構造(16)が考えられる 非縮合型構造と縮合型構造の割合は, 核磁気複雑共 リグニン分子中でフェニルプロパンはエーテルおよ構造式についてです。 アンモニアの構造式は、 hーnーh │ h ですが、nの下のhはnの上にきてもいいんですか? あと、構造式は分子式を元にして作られらてるのですか?
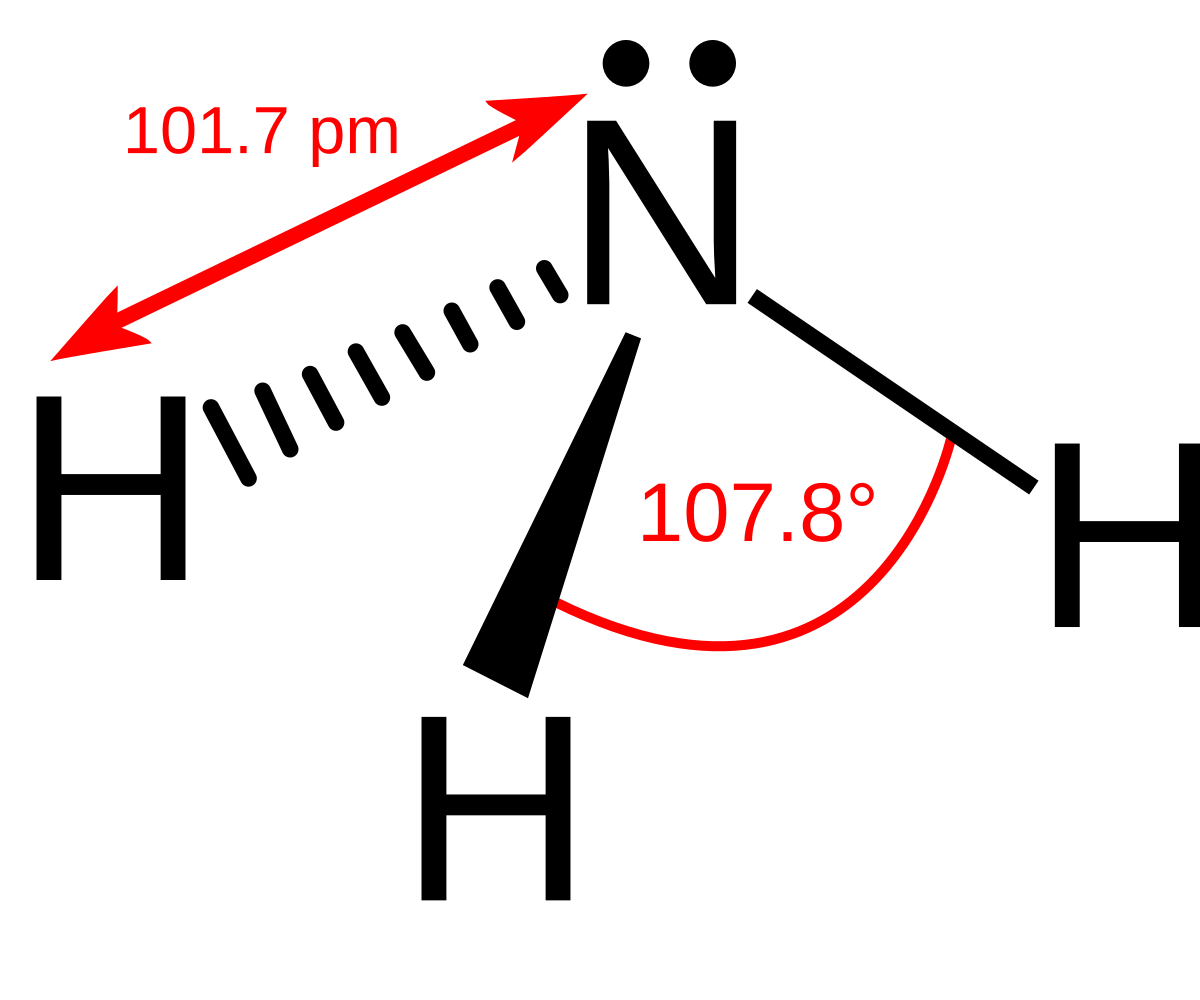
アンモニアにおける三角錐形幾何配置 編集 アンモニア中の窒素原子は5個の価電子と3つの水素原子との結合を持ち、オクテット則を満たしている。 この結果、それぞれの結合角が cos −1 (− 1 / 3) ≈ 1095° と等しい正四面体の幾何配置がもたらされるだろう。 。しかしながら、3つの水素原子高分子化学(Kebunshi Kagaku),Vol29,No332,pp(Dec,1972) NMRに よるアンモニアレゾールの数平均構造の決定 (受付1972年6月9日 ・掲載決定1972年8月21日)分子構造 この物質は式nh ヒドロキシルアニオンとアンモニウムカチオンとの相互作用の過程で、アンモニア分子が再び形成され、そのモル質量は17g / molであり、水分子も同様である。 それらが互いに相互作用すると、粒子は水素結合によって結合さ


分子構造ラバーマスコットbc 3 アンモニア Nh3 ネコポス不可 C トイサンタ Paypayモール店 通販 Paypayモール



魅惑のプルシアンブルーに秘められた 未来を変えるチカラ 深川 峻太郎 ブルーバックス編集部 ブルーバックス 講談社 3 4
アンモニア水中でのアンモニア分子の状態は、種々の実験事実から水酸化アンモニウムnh 4 ohの存在は考えられず、水分子の付加したnh 3 ・h 2 oとnh 4 ohの中間状態にあるものとされている。したがってアンモニアの水溶液を水酸化アンモニムのようによぶのは序になっているのはなぜでしょうか? これは分子構造 から合理的に説明できます。アミンの塩基性の強さは、 窒素原子上の非共有電子対の濃度 (電子密度) に関係 します。エチルアミンがアンモニアより塩基性が強い(ウ) 分子と共有結合 分子からなる物質の例として、代表的な無機物質については、水素、酸素、窒素、塩化水素、水、アンモニア、二酸化炭素などを扱う。



目で見て操作する 分子の世界 そのミクロ構造と物性 分子の構造



極性 分子の形との関係 求め方 打ち消しなどを例を用いて解説 化学のグルメ
分子式及び分子量 AlK(SO 4) 2 ・12H 2 O= AlNH 4 (SO 4) 2 ・12H 2 O= 無色正八面体の結晶、大気中では表面が風化して半透明になる。 比重/融点/比熱 比重(175) 融点(925℃) 比熱(03cal/g) 比重(164) 融点(935℃) 比熱(03cal/g)1 主な星間分子の スペクトル線 星間分子 生成=衝突 㱻 破壊=光解離 (紫外線) HI雲の密度が n(H)~102 cm3 になると、十部内部 (Av㸠1) ではダストによる減 光が効き、一度できた分子は星間紫外線で解離せずに存在できるようになるこの様なアンモニアの性質がどこからくるのか? 分子構造にさかのぼって考えてみたいと思います。 アンモニアの電子配置と電荷分布図 アンモニアの電子配置を図101に示します。 窒素原子に3個の水素原子が共有結合しています



アンモニアを窒素へ変換する触媒 Chem Station ケムステ


分子と共有結合 化学コラム
PV法による水とアンモニアの分離機構の一端が明らかになったことにより、水とアンモニアを高度分離することができる膜を開発することが可能になるであろう。 図1 キチン、キトサン及びセルロースの化学構造 図2 キトサン膜の脱アセチル化度と分子式 融点/℃ 沸点/℃ メタン,アンモニア,水 メタン(methane) ─ CH アンモニア(ammmonia) $ NH 水(water) $ H 2 O 0 氷構造の例 氷構造の例(n=4) 氷構造の例(n=28) 参考:極性・無極性を考えるために 酸素 塩化水素 二分子構造と結合(IV) 単純な原子価結合法でのアンモニア(NH 3)分子 窒素原子の電子配置:(1s) 2(2s) (2p)3 1s電子は,内殻なので結合に関与しない


ハーバー ボッシュ法を超えた 新たなアンモニア合成法が開発 財経新聞


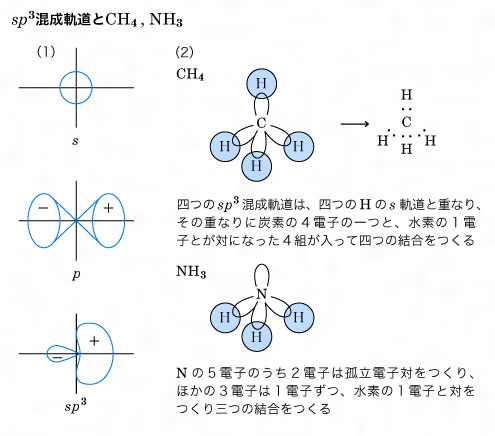
混成軌道
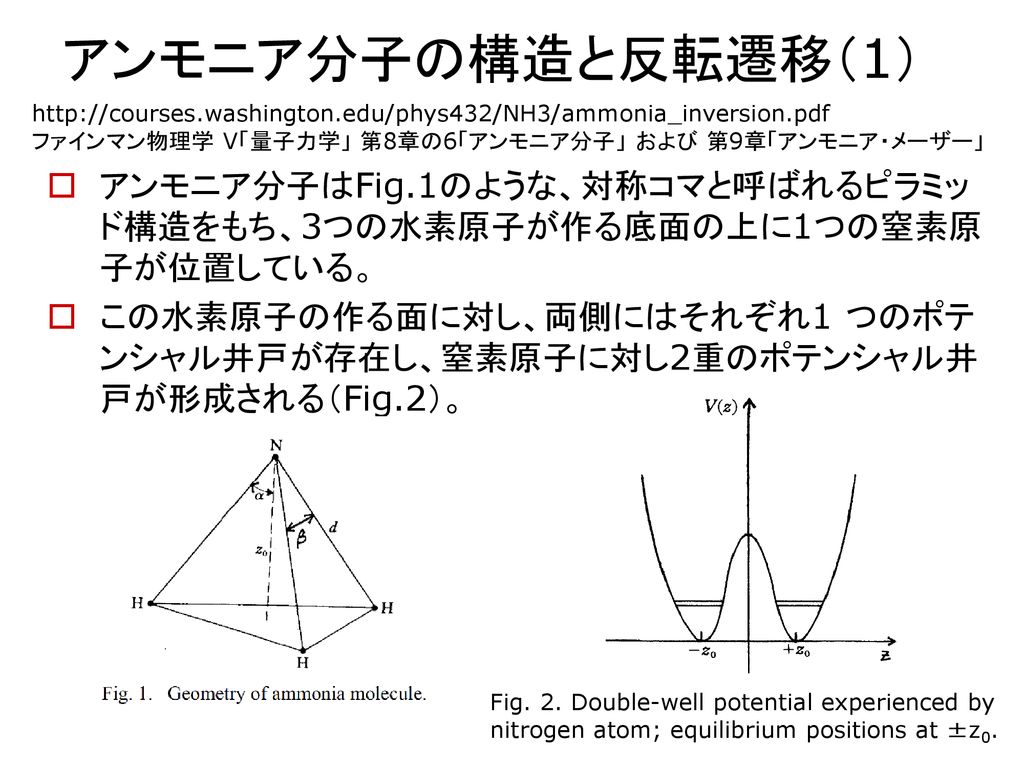
アンモニアの分子は、窒素原子1つと水素原子3つが図のように結合しています。この構造は、NH 3 と略すことが多いです。 「連結器」が1つある水素原子が3つ、「連結器」が3つある窒素原子と結合しているのです。 Challenge Quizしかし、分子構造の細かい部分については、混成軌道の理論だけでは説明できません。 例えば、アンモニア NH 3 分子の形は、近似的な sp 3 混成軌道として説明することができますが、 H N H 間の角度は理想的な角度である 1095° ではなく、 1075° と少し図1)は、星間空間で最初に(1968年)検出された 多原子分子である。 アンモニア分子は周波数 23 24 ghz の電波領域に多くの輝線をもち、 それらを使ってガスの温度や



なぜ水分子の構造は折れ線型なのか その理由を暴露 化学受験テクニック塾



メタンが無極性分子であり アンモニアが極性分子である理由 電気陰性度との関係
子や分子のスペクトルの研究が始まりました.これが マイクロ波分光学です. まずアンモニア分子の24GHz付近の多数のスペク トル線,次に水分子のGHzのスペクトル線が 観測されました.原子ではナトリウムで1772GHz,分子構造 (ぶんしこうぞう、molecular structure、molecular geometry)とは、 分子 の 幾何学 的構造をいい、例えば 原子 間距離や 配向 などをさす。 分子構造を調べるには、主に回折法と 分光法 が用いられる。 表 話分子 分子とは いくつかの原子が固く結びついた粒子を分子という。 分子はその物質の性質を示す最小の粒子である。 19世紀アボガドロが「気体は2個以上の原子が集まった分子でできている」と提唱した。 (現在では気体だけでなく固体や液体でも分子



共有結合を即理解 わかりやすい図で解説 高校生向け受験応援メディア 受験のミカタ


アンモニアとは コトバンク
して29eV 付近の構造はメタン分子二電子励起状態(主にD2 state)に起因すると考えら れる。さらに、アンモニアのLymanα けい光放出断面積(Fig2(b))との比較から、アンアンモニア分子の反転遷移に関する超微細構造線のJ=K=28状態についてのひん度測定 Frequency measurements of hyperfine structure lines for inversion transitions of the ammonia molecule for the states J=K=28 Bull Acad Pol Sci Ser Sci Chim (Bulletin de l'Academie Polonaise des Sciences分子の立体構造 覚え方 電気陰性度と分子の形、極性 皆さんは、水分子が折れ線型でアンモニアが三角錐型で、〇〇はーーと暗記してしまって居ませんか? 電気陰性度と電子対の考え方を使えば、極性の有無や分子の立体構造、更に水に溶けるのか


化学講座 第7回 分子性物質 私立 国公立大学医学部に入ろう ドットコム
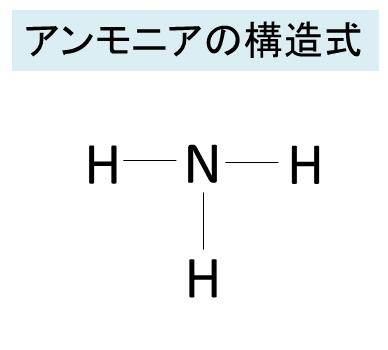


アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は
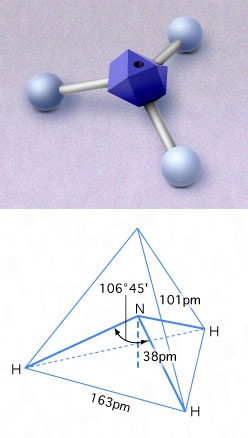
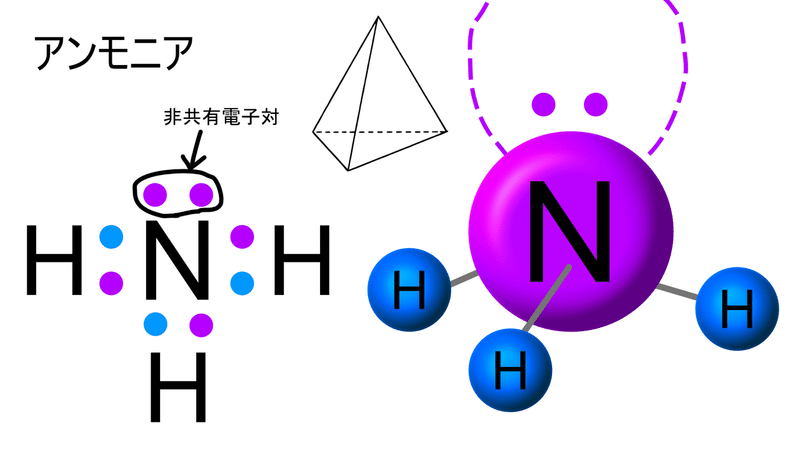
アンモニア分子はFig1のような、対称コマと呼ばれるピラミ ッド構造をもち、3つの水素原子が作る底面の上に1つの窒 素原子が位置している。 !典型的な三角錐構造を持つ分子の結合角は109ですが 孤立電子対の存在により、アンモニア分子の結合角は107°に減少しました。 図1アンモニアの化学構造 アンモニアの融点は7773です cと沸点は約3334です アンモニアは水分子と水素結合を形成する能力素材登録番号: a 素材名:多原子分子 アンモニアの分子構造(教室JPEG) アンモニアについても中心の窒素原子にsp3混成が起こっている。アンモニアの分子構造について解説。


名城大学理工学部応用化学科 永田研究室 有機化学基礎 第3回 疑問点など
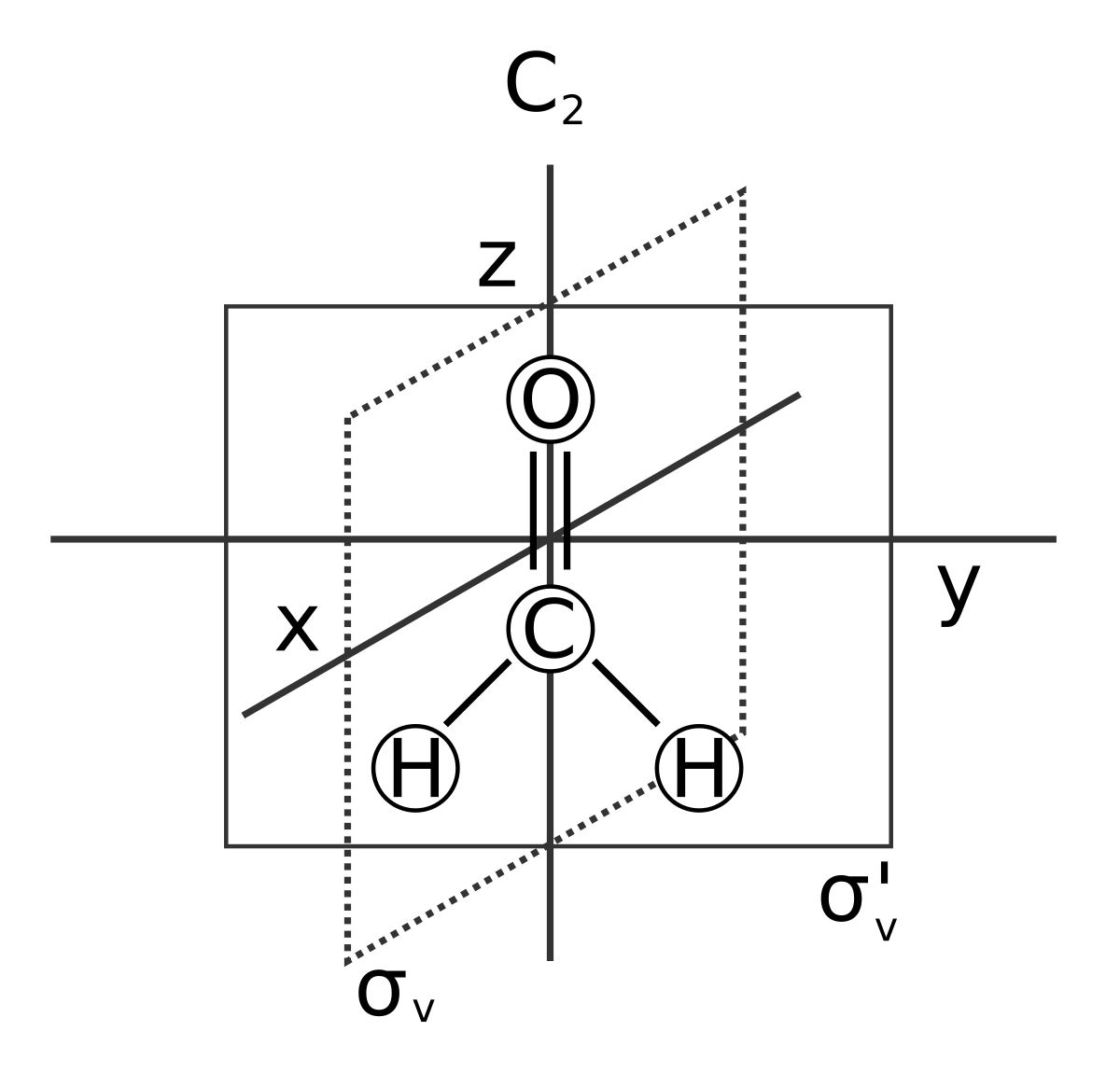


分子対称性 Wikipedia
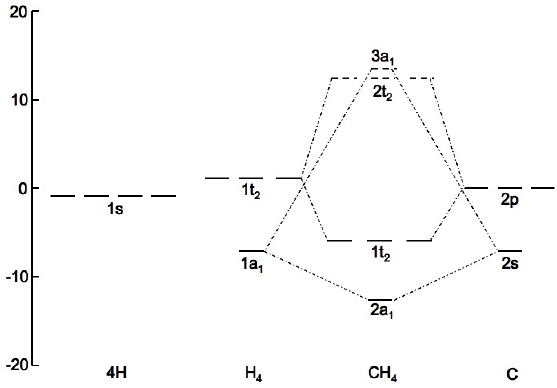
分子の形と電子状態 等核2原子分子の電子状態 等核2原子分子の分子軌道 H 2 H H 1s σ σ∗ 2 AO Molecular Orbitals AO MO Energy 水素分子の分子軌道と原子軌道との関係 ∆ε H 2 Formation energy ∆ E Bond Order (BO) H 2 H 2He 2 He 2 valence electrons 2 1 3 4 32 ∆ε∆ε∆ε 0∆ε 1



電子対の数から考える分子の形 Vseprモデル



アンモニアを窒素へ変換する触媒 Chem Station ケムステ
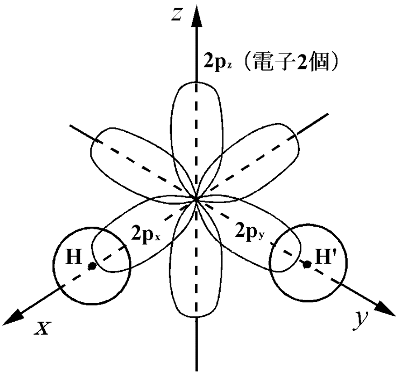


14 多原子分子


原子の手



アンモニア分子と構造式のイラスト素材 ベクタ Image



アンモニアと窒素のところの問題で 答えと少し違うのですがマルになりますか Clear
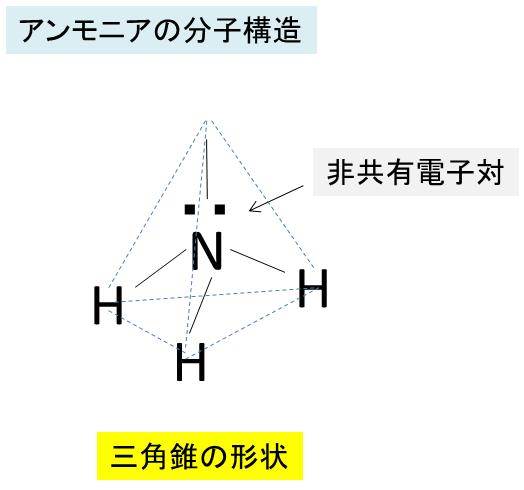


アンモニアの分子の形 立体構造 が三角錐 四面体 になる理由は 三角錐と正四面体の違いは アンモニアの結合角は107度



化学物質 分子 Nh3 アンモニア 構造 Ammonia 化学物質 分子 構造 Canstock


アンモニア You Iggy


大学化学への梯 なんで水分子は折れ線形なの Vsepr理論の基礎 やまたく Note



魅惑のプルシアンブルーに秘められた 未来を変えるチカラ 深川 峻太郎 ブルーバックス編集部 ブルーバックス 講談社 3 4



アンモニウム Wikipedia



分子 アンモニア Nh3 分子 隔離された Nh3 白 アンモニア 3d Canstock


化学講座 第7回 分子性物質 私立 国公立大学医学部に入ろう ドットコム



水素 水 アンモニア メタンの化学式と分子モデル ベクトル図のイラスト素材 ベクタ Image



水素水アンモニアメタンの化学式と分子モデル化学学校ノートブック檻の中の紙のシート 3dのベクターアート素材や画像を多数ご用意 Istock


分子からの放射 河野孝太郎 平成26年 基礎天文学観測実習 電波望遠鏡による分光撮像観測 実習配布資料からの抜粋 Ppt Download



高校化学基礎 分子の形 映像授業のtry It トライイット



Lihat Cara Penyelesaian Di Qanda



Amazon 分子構造ラバーマスコットbc 3 アンモニア Nh3 単品 ガチャガチャ カプセルトイ ぬいぐるみ おもちゃ



アンモニアの電子式から構造式を考えるときに 非共有電子対は無視していいんですか Clear



電子対の数から考える分子の形 Vseprモデル



化学物質 分子 Nh3 アンモニア 構造 Ammonia 化学物質 分子 構造 Canstock


4章b 類題1 1 Top B 問題 次文を読んで下の各問いに答えなさい 物質は元素記号を用いて化学式で表わすことが多い その化学式には 示性式 構造式 分子式 電子式および組成式などがある 例えば A酢酸は 示性式 構造式 分子式 電子式および


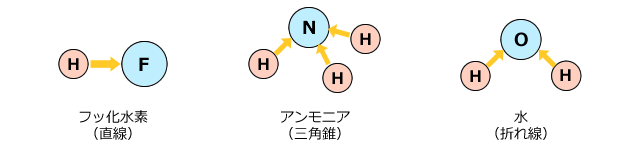
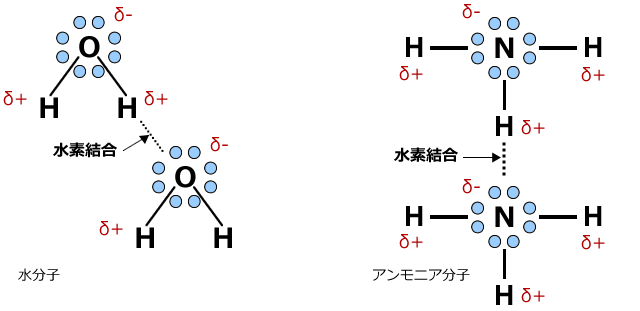
化学 水素結合と分子の凝集 技術情報館 Sekigin 水 フッ化水素やアンモニアの沸点 融点の異常を説明する水素結合と分子の凝集 会合状態 を紹介


アンモニア結晶構造のイラスト素材


アンモニア Wikipedia



アンモニアを室温以下で分解できる触媒について Chem Station ケムステ



化学基礎 配位結合 その2 結合と構造 Youtube


電波天文学教材


アンモニア分子の成り立ちについて電子配置 電子式 構造式 分子の形を示しつつ Yahoo 知恵袋



アンモニアnh3分子モデル化学式 3dのベクターアート素材や画像を多数ご用意 Istock


71 C Lihat Cara Penyelesaian Di Qanda
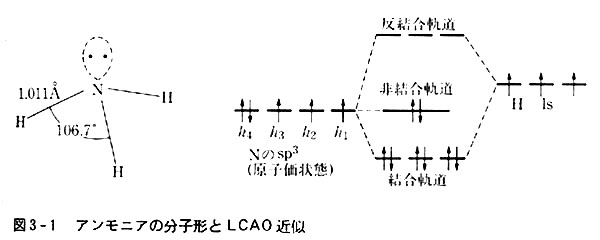


2 分子内結合の近似 非金属原子間の共有結合をlcao法で近似する方法はp 32に述べたが それを種々な分子に適用した場合を考察する 1 非結合対を生じる場合 図3 1にはアンモニアnh3のlcao近似を示した 分子構造は図示のとおりで3個の



電子対の数から考える分子の形 Vseprモデル


第7章 分子の形と極性



アンモニウム 正荷電の多原子イオンの 3 D 構造 それはアンモニア分子のプロトン化によって形成されます 正荷電のアンモニウムはまた一般的な名前またはプロトン化置換アミン の写真素材 画像素材 Image



電子対の数から考える分子の形 Vseprモデル


化学 分子 分子とは 種類 アンモニア


アンモニア分子構造のランディングページ プレミアムベクター



化学 折れ線形と三角錐形と正四面体形と直線型の違い 雑記


Llyovsl Ddbswm



アンモニア二酸化炭素酸素水素分子構造式イラスト No 無料イラストなら イラストac



極性分子と無極性分子のを見分ける方法 2つの知識で見分けられます 化学受験テクニック塾


化学 水素結合と分子の凝集 技術情報館 Sekigin 水 フッ化水素やアンモニアの沸点 融点の異常を説明する水素結合と分子の凝集 会合状態 を紹介
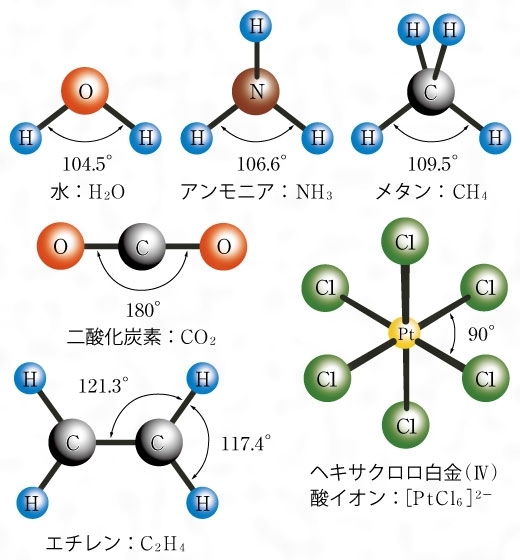


結合角 ケツゴウカク とは コトバンク
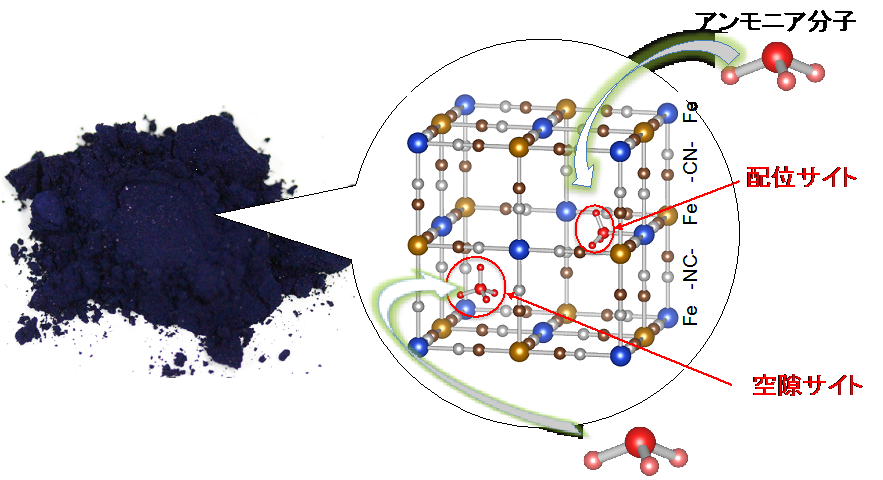


青色顔料が高性能アンモニア吸着材であることを発見 東京大学 大学院理学系研究科 理学部



Chem Chem Cher Ee Rhf 3 21gレベルにおけるアンモニアの構造最適化 振動解析
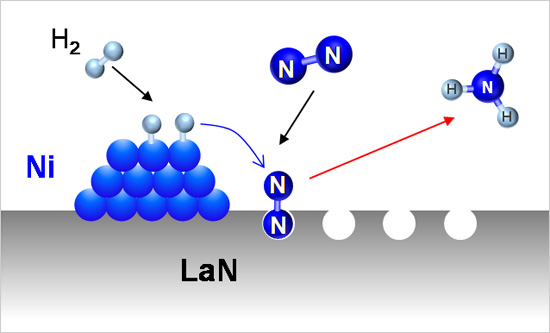


ニッケル触媒のアンモニア合成活性 窒素空孔の形成されやすさが鍵 Nims



共同発表 貴金属使わずアンモニア合成触媒となる新物質発見


第15族元素 窒素族元素


化学構造式 Chemsketch ケムスケッチ の裏技5選 非共有電子対の描き方など 使い方 化学ネットワーク 化学解説 業界研究 就職



アンモニア Nh3 化学 3 Pixabayの無料画像



メタン Ch4 の形が正四面体である理由 結合角は109 5度


酸化還元反応 電子のやり取り


10章 アンモニアの性質


茨城大学 宇宙科学教育研究センター


72x N A Lihat Cara Penyelesaian Di Qanda


共有結合分子の構造を知るためには Juke 99 Note


メタン分子ch4



化学基礎 立体構造について 分子の構造についてです 非共有電子対 化学 教えて Goo



錯イオンの配位数と立体構造まとめ Irohabook



フロン排出抑制法 Eラーニングシステム Meti 経済産業省
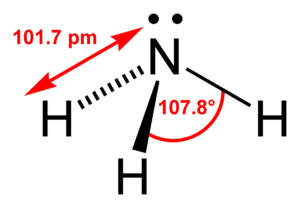


6月24 26日学習ログ アンモニアと塩化水素はなぜ水によく溶けるのか 翻訳のアシオト


アンモニア 分子 Icon バックグラウンド 分子 Illustration アンモニア アイコン 白 ベクトル Canstock



高校化学基礎 分子の形 映像授業のtry It トライイット



58 Lihat Cara Penyelesaian Di Qanda


自由運動するアンモニア分子 3dのイラスト素材
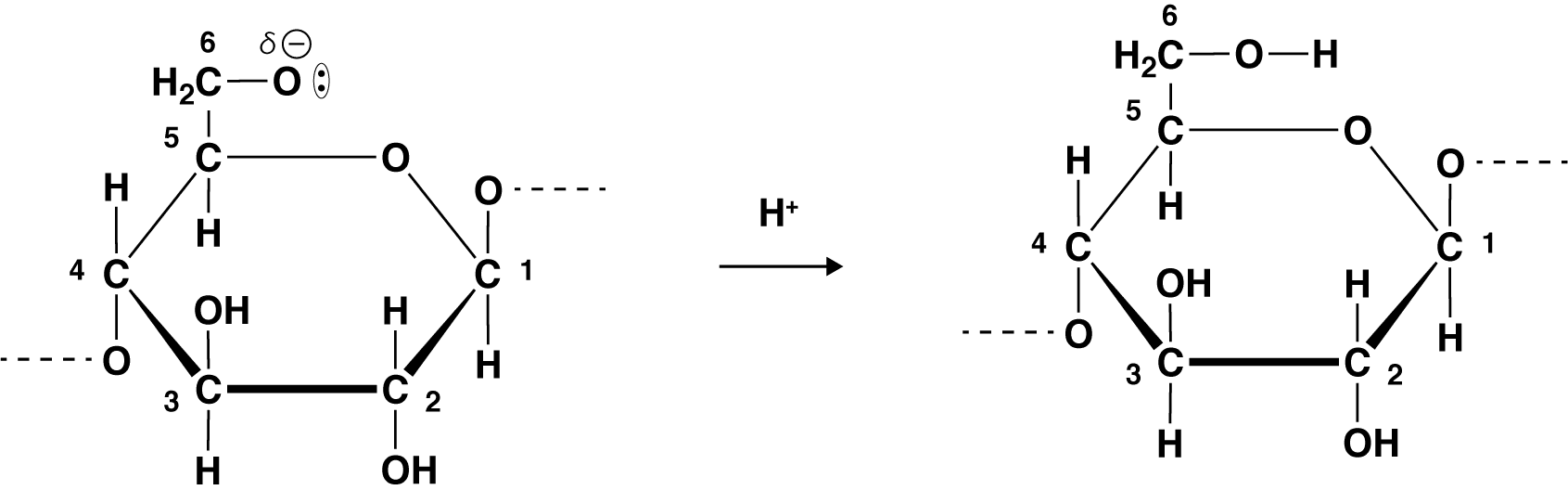


ビスコースレーヨン 銅アンモニアレーヨン 作り方 原理 構造式 用途など 化学のグルメ
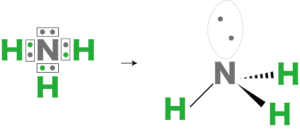


極性 分子の形との関係 求め方 打ち消しなどを例を用いて解説 化学のグルメ


化学結合とは コトバンク
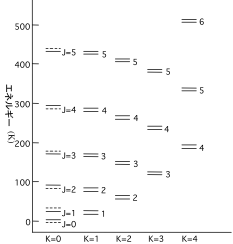


電波天文学教材



大学の有機化学 骨格構造式を描くときのルール 理系のための備忘録
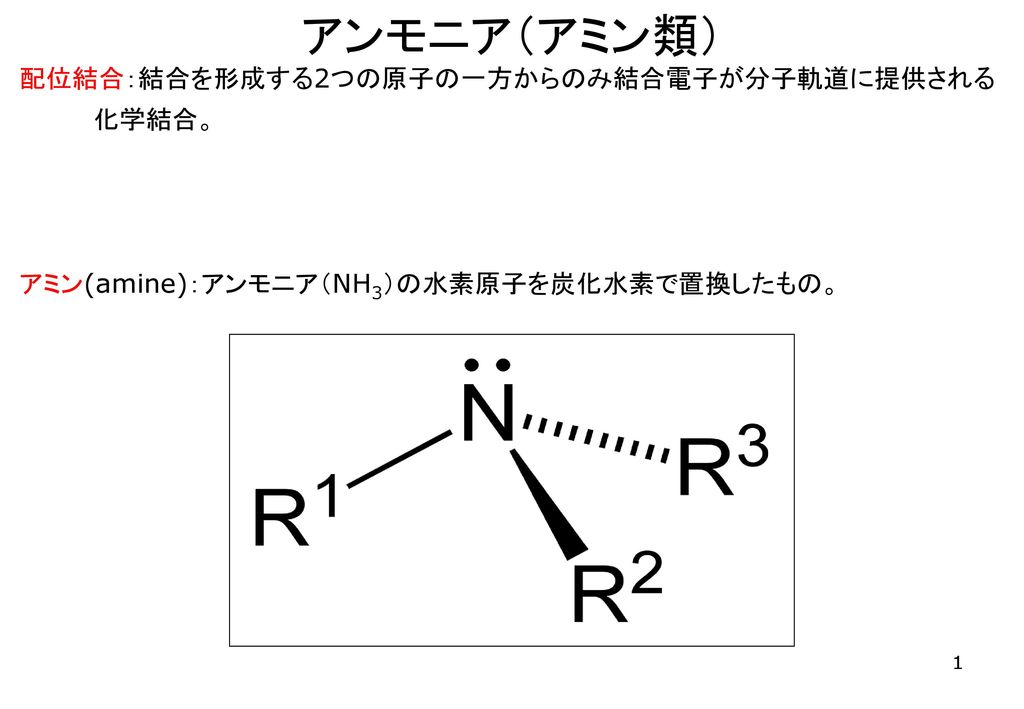


アンモニア アミン類 配位結合 結合を形成する2つの原子の一方からのみ結合電子が分子軌道に提供される化学結合 Ppt Download
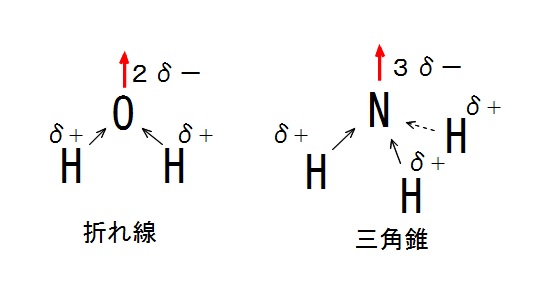


電気陰性度の大きさと分子の極性



アンモニア とは 意味 エキサイト辞書



電子対の数から考える分子の形 Vseprモデル
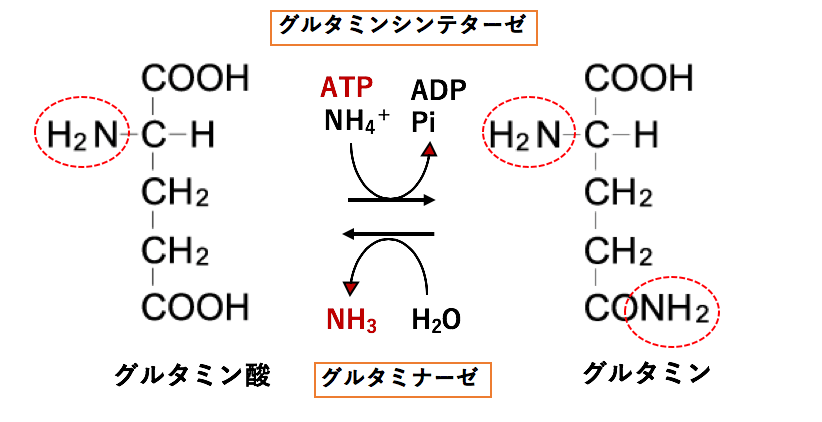


解決 グルタミン酸とグルタミンを介したアンモニアの体内輸送


10章 アンモニアの性質
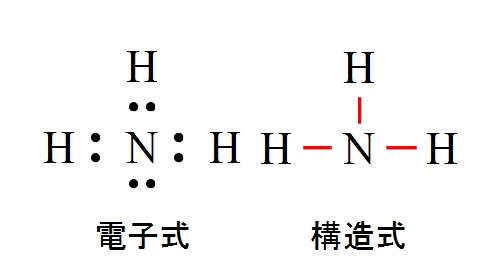


共有結合の種類と分子の形と結晶



Amazon 分子構造ラバーマスコットbc 全5種セット フルコンプ ガチャガチャ カプセルトイ カプセル玩具 おもちゃ


混成軌道
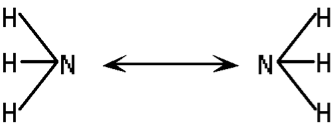


電波天文学教材


0 件のコメント:
コメントを投稿